Ultima modifica il 31 März 2026
Hinweis: Der Bericht wurde vom Unterzeichner bewusst anonymisiert, indem die Namen der Ärzte entfernt wurden
Lugano, 02. April 2021/sc
INTERNER VERLEGUNGSBERICHT
| Achermann Mirko, Via Contrada San Marco 31a, Agno – 05.04.1967 |
Sehr geehrter Kollege,
hiermit informieren wir Sie über den oben genannten Patienten, der vom 31.01.2021 bis zum 25.03.2021 auf unserer Intensivstation stationär behandelt wurde.
Diagnose:
- Schweres ARDS bei beidseitiger SARS-CoV-2-Pneumonie, Variante N501Y (Erstdiagnose 07.01.2021):
- Veno-venöse extrakorporale Membranoxygenierung (ECMO) vom 31.01.2021 bis 18.02.2021; Zyklen der Bauchlagerung vom 20.02.2021 bis 22.02.2021;
- Thorax-CT (Clinica Moncucco, 23.01.2021): diffuse beidseitige Infiltration, progredient im Vergleich zur Untersuchung vom 13.01.2021, keine Anzeichen für Lungenembolien.
- Nativ-CT des Thorax (08.02.2021): Auftreten von Parenchymkonsolidierungen mit bronchiektatischen Veränderungen in den Unterlappen, Verdacht auf SOP (schwere organisierende Pneumonie). Im verbleibenden Parenchym zeigt sich eine geringere Intensität der Milchglasveränderungen im Vergleich zu den vorangegangenen Kontrollen vom 23.01.2021.
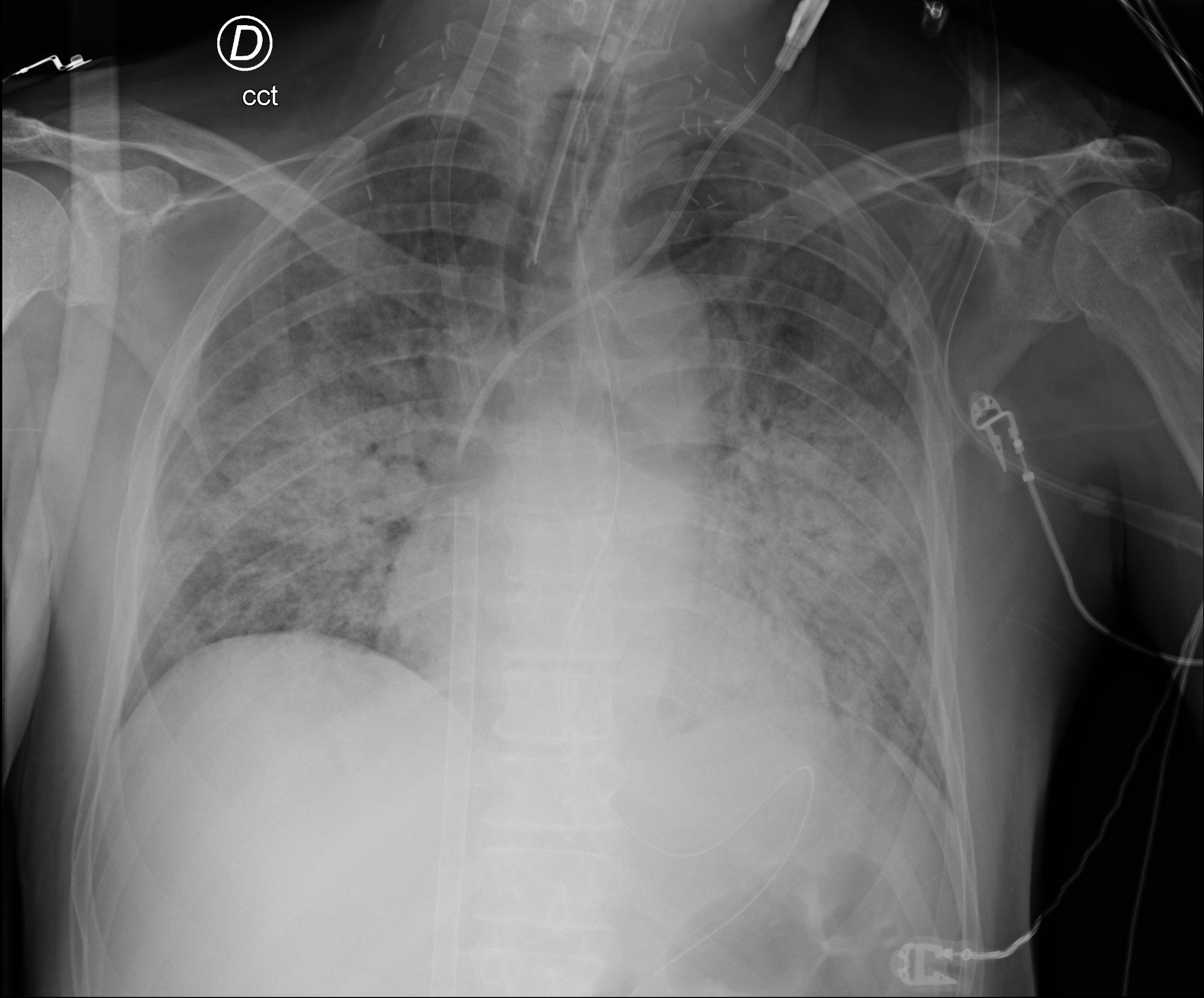
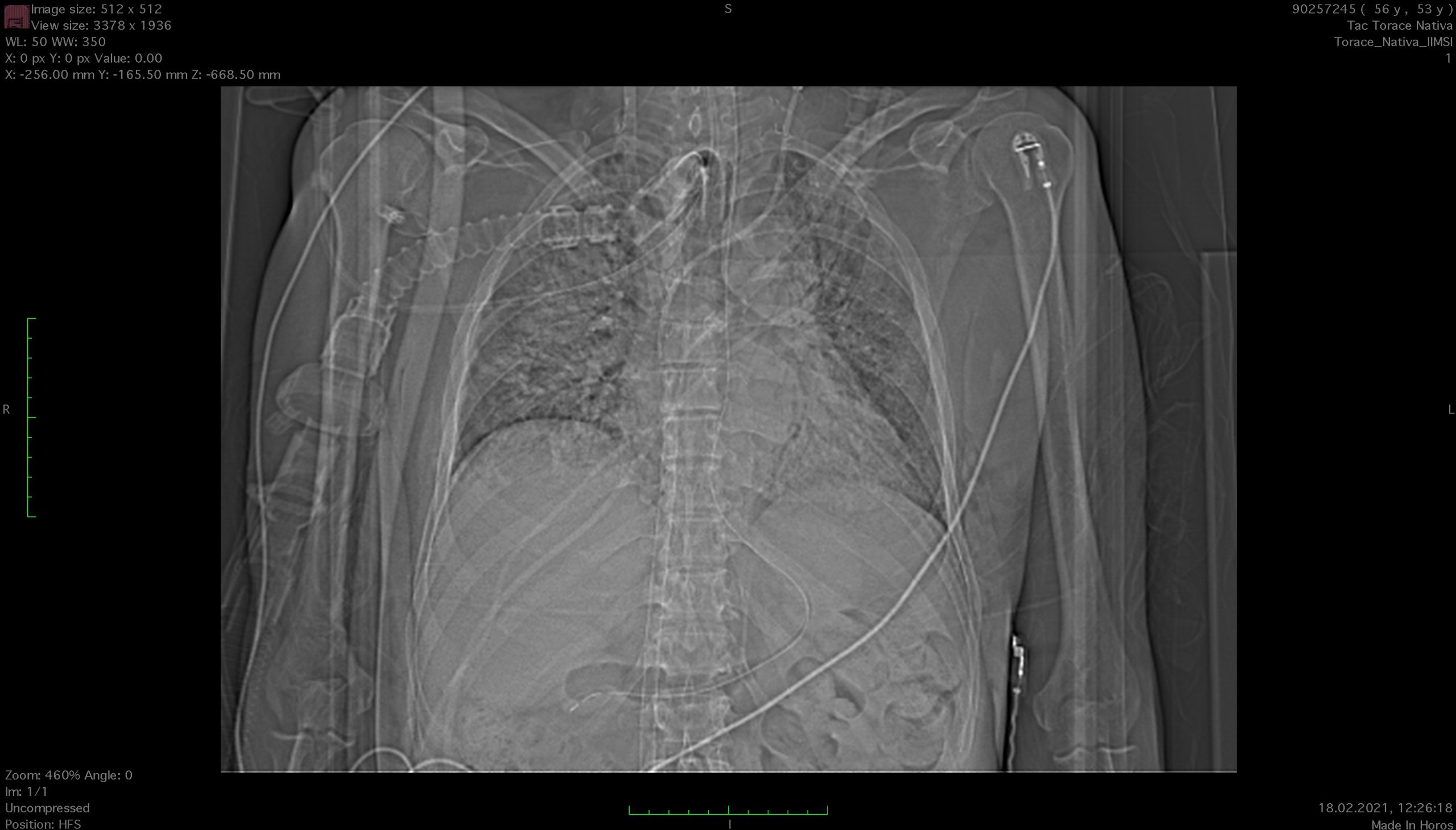
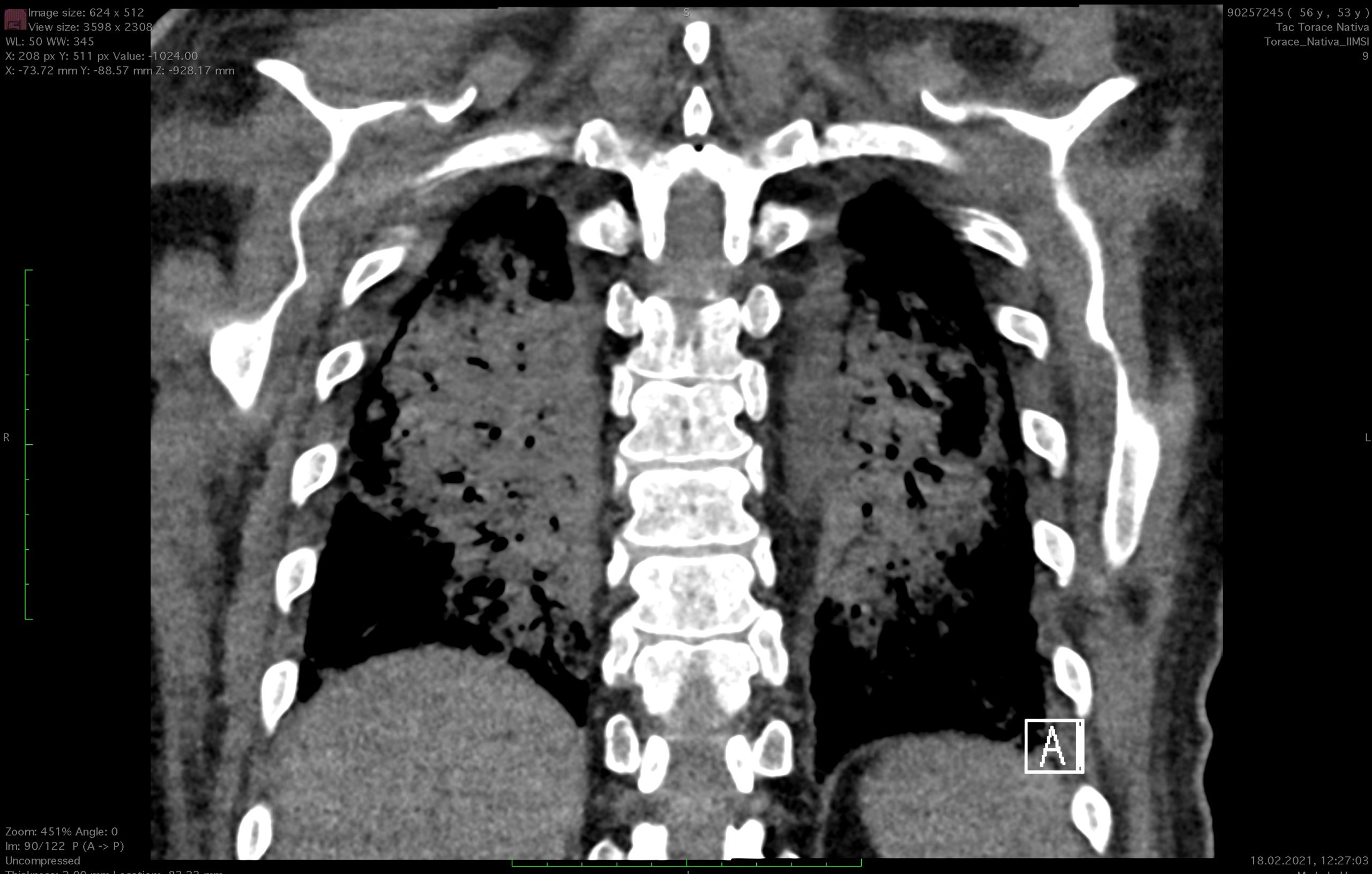
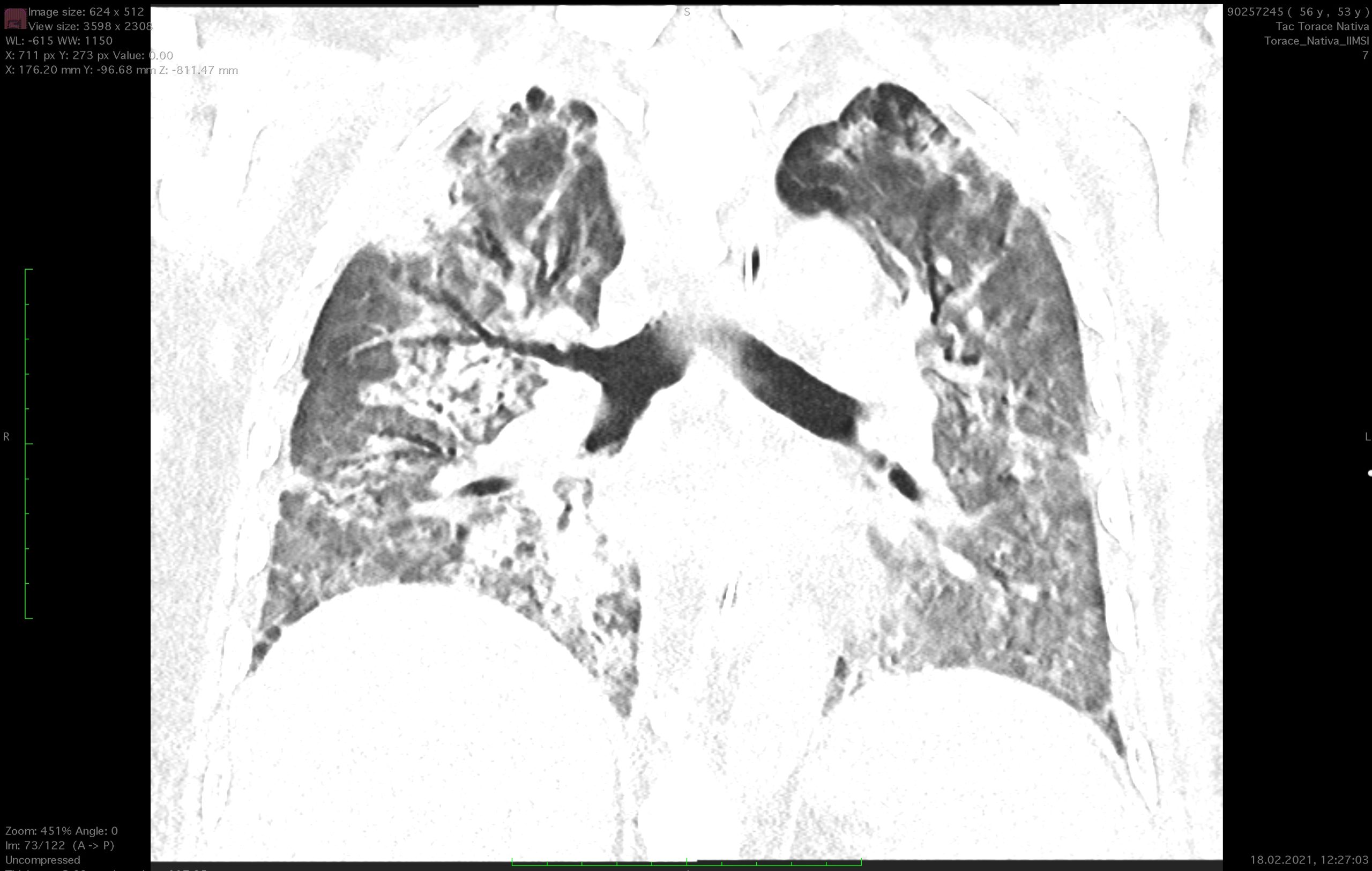
Röntgenaufnahme vom 01.02.2021 um 00:14:56 Uhr bei meiner Aufnahme auf der Intensivstation des Cardiocentro Ticino - Nativ-CT des Thorax (18.02.2021): auf Parenchymebene größere Milchglasareale und Zunahme beidseitiger Konsolidierungszonen in den hinteren Segmenten der Ober- und Unterlappen. Aspirationsphänomene über die Tracheostomie.
- Thorax-Abdomen-CT (01.03.2021): Verbesserung des Lungenbildes im Vergleich zur Voruntersuchung, wobei kleine beidseitige Infiltrate in der Peripherie bestehen bleiben. Diffuse veränderte Dämpfung des Lungenparenchvms, wahrscheinlich im Sinne einer Erkrankung der kleinen Atemwege.
- Nativ-CT des Thorax (15.03.2021): Befund unverändert im Vergleich zur Voruntersuchung vom (01.03.2021) mit persistierenden kleinen peripheren Infiltraten beidseits. Diffuse veränderte Parenchymdämpfung, wahrscheinlich im Sinne einer Erkrankung der kleinen Atemwege.
- SARS-CoV-2
- PCR-Nasen-Rachen-Abstrich (01.02.2021): positiv; Serum-IgM negativ / Serum-IgG positiv (10.02.2021); Mutation N501Y (01.02.2021): positiv
- PCR aus BAL (09.02., 11.02.2021): negativ
- Stuhl-PCR (14.02.2021): negativ
- Actemra am 16.01.2021 (Clinica Moncucco)
- Dexamethason 6 mg vom 22.01. bis 31.01.2021 (Clinica Moncucco)
- Solu-Medrol 80 mg ab dem 31.01.2021, schrittweise ausgeschlichen bis zum 23.02.2021; Immunmodulation mit Spironolacton und Azithromycin vom 09.02.2021 bis 19.02.2021
- Boost-Corticotherapie mit Solu-Medrol 1 g/Tag (24.–26.02.2021), 500 mg/Tag (27.02.–01.03.2021)
- Solu-Medrol 50 mg/Tag (ab 02.03.2021)
- Transthorakale Echokardiographie (10.03.2021): Größe des linken Ventrikels im Normbereich. Globale systolische Funktion erhalten (EF 55–60 %). Linker Vorhof normal groß. Trikuspide Aortenklappe, normal funktionierend. Minimale Mitralinsuffizienz. Rechter Ventrikel normal groß und normal beweglich. Vena cava inferior nicht erweitert, normal kollabierend. Aortenbulbus (38 mm) und proximale Aorta ascendente (35 mm) normal groß. Kein Perikarderguss.
- Multifaktorielle globale respiratorische Insuffizienz im Rahmen von Ad1, ventilatorassoziierte Pneumonie und Intensivstation-Myopathie:
- Anlage einer perkutanen Tracheostomie am 11.02.2021
- Revision der Tracheostomie am 12.02. und 13.02.2021; Bronchoskopie am 13.02.2021 und 16.02.2021
- Invasive Beatmung vom 31.01.2021 bis 23.03.2021
- Bakteriämie durch Klebsiella pneumoniae bei ventilatorassoziierter Pneumonie (VAP):
- Antibiotische Therapie: Piperacillin-Tazobactam vom 23.01. bis 31.01. (Clinica Moncucco); Meropenem vom 01.02. bis 10.02.2021, Ceftriaxon vom 10.02. bis 14.02. 2021.
- Ventilatorassoziierte Pneumonie (VAP) durch Enterococcus faecalis (bronchoalveoläre Lavage (11.02.2021):
- Cefepim vom 15.02. bis 20.02.2021.
- Bakteriämie durch Enterococcus faecium unklarer Herkunft:
- Vancomycin vom 15.02. bis 22.02.2021; Linezolid vom 23.02. bis 04.03.2021.
- Fieberzustand unklarer Genese (FUO) DD: Schwere organisierende Pneumonie, medikamenteninduziert (Antihistaminika, Neuroleptika), Reaktivierung der CML unwahrscheinlich, Rebound nach Reduktion der Steroidtherapie
- Erworbene Immunsuppression unter hochdosierter Steroidtherapie:
- Prophylaktische Therapie mit Meropenem vom 20.02. bis 02.03., Therapie mit Co-Trimoxazol 3x/Woche ab dem 01.03.2021.
- Koagulopathie multifaktorieller Genese mit Anämie und Thrombozytopenie:
- Mechanische hämolytische Komponente unter ECMO oder Verbrauchskoagulopathie bei Blutungen, beginnende DIC
- Thrombozyten-Nadir bei 70 G/l am 13.02.2020
- Gabe von 20 Erythrozytenkonzentraten, 3 Thrombozytenkonzentraten, 4 Einheiten gefrorenem Frischplasma
- Schädel-CT (18.02.2021): keine hämorrhagischen Läsionen oder densitometrischen Veränderungen erkennbar. Blutung aus der Tracheostomie, die eine chirurgische Revision erforderte (12.02. und 13.02.2021)
- Schwere Intensivstation-Myopathie mit beginnender neuropathischer Komponente:
- Begünstigt durch hochdosierte Steroidtherapie
- Elektroneuromyographie (11.03.2021): axonale Degeneration des Nervus peroneus beidseits ohne weitere Anzeichen von Neuropathien
- Gleichzeitige schwere Protein-Energie-Malnutrition (NRS 7).
- Hyperkinetisches Intensivstation-Delir
- Generalisierter Myoklonus mit Sakkaden/Augenflattern DD: Opsoklonus-Myoklonus-Syndrom:
- Verdacht auf Post-COVID-Myoklonus
- Neurologischer Status (Dr. Galati, 23.03.2021): wach, kooperativ, hypotone Sprache. Augenmotorik mit intrusiven Sakkaden. Diffuser Myoklonus, überwiegend Aktionsmyoklonus, gemischt positiv und negativ an Gesicht, Rumpf und Extremitäten (vorwiegend linke obere Extremität). Keine Defizite der Gesichtsmuskulatur. Kopfbeugung erhalten. Hebt beidseits die Schultern (M5-), Schulterabduktion beidseits M4-, rechtsbetonte Iposthenie. Diffus M3 an der rechten Extremität; an der linken Extremität diffus M4-. An den unteren Extremitäten Hüftbeugung und Beinstreckung beidseits M4; Plegie der Dorsalflexion des linken Fußes; Plantarflexion der Füße beidseits M4. Finger-Nase-Versuch links mit telekinetischem Tremor möglich. Rechts nicht beurteilbar und Knie-Hacken-Versuch aufgrund der Parese nicht beurteilbar. PSR/ASR: Trizepssehnenreflex rechts auslösbar; andere Reflexe erloschen. Pyramidenbahnzeichen: beidseitige Flexion.
- Schädel-MRT mit Kontrastmittel (24.03.2021): Befunde im Normbereich. Klinische Besserung unter Therapie mit Keppra.
- Schwere gemischte Dysphagie, begünstigt durch Intensivstation-Myopathie:
- Logopädisches Konsil (15.03.2021): vollständige Dysphagie für feste und flüssige Stoffe, Hustenanfälle mit Austritt von paratrachealem Sekret
- Logopädisches Konsil (16.03.2021): Schluckakt weiterhin ineffektiv, Vorhandensein von Hustenanfällen mit paratrachealem Sekretfluss
- Logopädisches Konsil (18.03.2021): Besserung des Schluckaktes, gelegentliche Hustenanfälle bei Wassergabe
- Logopädisches Konsil (22.03.2021): bei Schluckversuchen mit festen und flüssigen Stoffen keine Dysphagie mehr. Umstellung auf passierte Dysphagie-Kost mit nicht angedickten Flüssigkeiten und zerkleinerten Medikamenten.
- Chronische myeloische Leukämie in der chronischen Phase:
- Diagnose 28.09.2020
- Peripherer Blutausstrich (23.09.): Ausgeprägte Neutrophilie, zahlreiche myeloische Vorstufen bis hin zu seltenen zirkulierenden Blasten beobachtet. Basophilie und Eosinophilie
- Knochenmarkaspirat (28.09.2020): Mark mit erhöhter Zellularität, gekennzeichnet durch eine Hyperplasie der myeloischen Reihe, assoziierte Eosinophilie und Basophilie, ohne Blastenüberschuss (2,8 % der Gesamtzellularität). Immunphänotyp: CD34+-Elemente entsprechen 0,6 % der Gesamtzahl
- Beckenkammbiopsie (28.09.2020): histologischer Befund vereinbar mit myeloproliferativer Neoplasie vom Typ chronische myeloische Leukämie; Anteil der CD34+-Blasten unter 5 % der Zellularität
- Zytogenetik: 46, XY, t(9;22)(q34;q11.2)[23]
- Molekularbiologie: BCR/ABL1-Fusionsgen b3a2 (p210) vorhanden
- Abdomensonographie: Leber mit homogener Echostruktur, normal in Größe, Grenzen und Rändern. Milz vergrößert (15,5 cm). Risiko-Scores: Sokal niedrig (0,7), Hasford niedrig (728,54), EUTOS niedriges Risiko (46).
- Laufende hämatologische Therapie: Imatinib 400 mg 1x/Tag seit 03.10.2020. Unterbrochen vom 31.01.2021 bis 12.03.2021 auf hämatologische Indikation. Wiederaufnahme am 12.03.2021
- Peripherer Blutausstrich (03.03.2021): Anämie mit Retikulozytose, vereinzelte Dakryozyten beobachtet, Neutrophilie mit seltenen myeloischen Vorstufen bis hin zu einem isolierten Blasten
- Peripherer Blutausstrich (15.03.2021): neutrophile Leukozytose, Neutrophile mit toxischen Zeichen, myeloische Vorstufen bis hin zu einem isolierten zirkulierenden Blasten beobachtet. Befund im Rahmen der bekannten CML und eines reaktiven Zustands einzuordnen.
Nebendiagnosen:
- Allergisches Asthma
- Beidseitiges Thoracic-Outlet-Syndrom:
- Neurologische Symptomatik behandelt mit Resektion der ersten rechten Rippe über einen supraklavikulären Zugang mit Neurolyse des Plexus brachialis (18.01.2018)
- Neurologische Symptomatik behandelt mit Resektion der ersten rechten Rippe über einen supraklavikulären Zugang mit Neurolyse des Plexus brachialis (18.01.2018)
- Lumbosakrales Wurzelsyndrom L5 links:
- Zustand nach periradikulärer Infiltration L5 links (10.02.2020)
- Zustand nach Stabilisierung L5-S1 (Dr. med. Liverani, 2000)
- Zustand nach Stabilisierung L4-L5 bei Radikulopathie L5-S1 links, Entfernung des Osteosynthesematerials L5-S1, außer einer Schraube in S1 links (2009)
- Sigmoidektomie wegen Divertikulitis (2005)
Komplikationen:
Blutung aus der perkutanen Tracheostomie mit chirurgischer Revision am 12.02. und 13.02.2021.
Kardiovaskuläre Risikofaktoren:
keine.
Anamnese:
53-jähriger Patient, bekannt für die genannten Diagnosen.
In onkohämatologischer Behandlung wegen einer kürzlich diagnostizierten chronischen myeloischen Leukämie.
Am 07.01.2021 wurde mittels Nasenabstrich eine SARS-CoV-2-Infektion diagnostiziert, zunächst ohne Symptome.
In den folgenden Tagen trat eine zunehmende Dyspnoe auf, die ab dem 12.01.2021 eine Hospitalisierung in der Clinica Moncucco in Lugano erforderlich machte.
Der Patient war vom 12.01.2021 bis 19.01.2021 auf der Intensivstation und erhielt Zyklen nicht-invasiver Beatmung (NIV) sowie eine Einzeldosis Tocilizumab am 16.01.2021.
Zunächst auf die Innere Medizin verlegt, erfolgte die Rückverlegung auf die Intensivstation wegen einer respiratorischen Insuffizienz, die eine orotracheale Intubation vom 22.01. bis 29.01. erforderlich machte. 2021.
Gleichzeitig mit der Verschlechterung wurde eine Therapie mit Dexamethason ab dem 22.01.2021 für insgesamt 10 Tage eingeleitet sowie bei Verdacht auf eine pulmonale Superinfektion eine Therapie mit Piperacillin-Tazobactam bis zum 28.01.2021.
Er profitierte von Zyklen der Bauchlagerung und einer protektiven Beatmung.
Aufgrund des scheinbar günstigen Verlaufs wurde der Patient am 29.01.2021 extubiert.
Am 31.01. beobachteten die Kollegen eine erneute Verschlechterung des Gasaustauschs, die eine erneute orotracheale Intubation erforderlich machte.
Angesichts der fortschreitenden globalen respiratorischen Insuffizienz trotz invasiver Beatmung, mit respiratorischer Azidose und hohen Beatmungsdrücken, die nicht auf Bauchlagerungsmanöver ansprachen, wurde der Patient am selben Tag zur Anlage einer veno-venösen ECMO in unser Institut verlegt.
Verfahren:
- Veno-venöse extrakorporale Membranoxygenierung (ECMO) (rechts femoral-jugulär) vom 31.01. bis 18.02.2021;
- Mechanische Beatmung vom 31.01. bis 23.03.2021;
- Perkutane Tracheostomie am 11.02.2021, Prof. Dr. med. Tiziano Cassina: siehe Befund;
- Chirurgische Revision der Tracheostomie (12.02. und 13.02.2021);
- Bronchoskopie (13.02., 16.02.2021, Pneumologe OCL): siehe Befund;
- Thorax-CT (08.02., 18.02., 15.03.2021): siehe Befund;
- Schädel-CT (18.02.2021): siehe Befund;
- Transthorakale Echokardiographie (10.03.2021): siehe Befund;
- Thorax-Abdomen-CT (01.03.2021): siehe Befund;
- Elektroneuromyographie (11.03.2021): siehe Befund;
- Antibiotische Therapie:
- Meropenem (01.02.2021–10.02.2021)
- Ceftriaxon (10.02.2021–14.02.2021)
- Cefepim (15.02.2021–20.02.2021)
- Vancomycin (15.02.2021–22.02.2021)
- Linezolid (23.02.2021–04.03.2021)
- Meropenem (20.02.2021–02.03.2021)
- Prophylaktisches Co-Trimoxazol vom 01.03.2021 bis (3-mal wöchentlich);
- Blutkulturen (01.02., 12.02., 14.02., 19.02., 22.02., 27.02., 01.03., 05.03., 07.03.2021);
- Urinkulturen (01.02., 12.02., 01.03., 05.03.2021);
- Bronchoalveoläre Lavage (11.02., 22.02.);
- Bronchialaspirat (01.02., 04.02., 21.02., 28.02., 05.03., 08.03.2021);
- Legionellen- und Pneumokokken-Antigen im Urin (01.02.2021);
- Legionellen-PCR aus BAL (11.02., 22.02.2021);
- Aspergillus-Galactomannan im Serum (20.02., 05.03.2021);
- Aspergillus-Galactomannan im Bronchialaspirat (01.02., 11.02., 22.02., 05.03.2021);
- Strongyloides-Serologie (20.02.2021);
- Cytomegalievirus-PCR (04.02., 11.02., 22.02., 02.03.2021);
- Beta-Glucan-Bestimmung (01.02., 20.02.2021);
- Bronchialaspirat (22.03.2021);
- Untersuchung auf SARS-CoV-2-Infektion:
- Nasen-Rachen-Abstrich (01.02.2021)
- PCR aus BAL (09.02., 11.02.2021)
- Stuhl-PCR (14.02.2021)
- Serologie (10.02.2021)
- Transfusion von 18 Erythrozytenkonzentraten, 3 Thrombozytenkonzentraten, 4 Einheiten gefrorenem Frischplasma;
- Logopädisches Konsil (15.03., 16.03., 18.03., 22.03.2021);
- Schädel-Kernspintomographie (24.03.2021): siehe Befund.
Verlauf und Diskussion
Zu 1-2:
Bei Aufnahme Patient intubiert, unzureichender Gasaustausch bei respiratorischer Azidose und schwerer Hypoxämie.
Versuche, eine protektive Beatmung einzustellen, erwiesen sich als unwirksam, wobei die Plateaudrücke (Pplat) ohne Nutzen für die Oxygenierung über 30 mmHg blieben.
Nach kollegialer Diskussion wurde am 31.01.2021 die rasche Anlage einer veno-venösen ECMO (rechts femoral-jugulär) beschlossen.
Der chirurgische Eingriff verlief ohne Besonderheiten.
Infektiologisch (siehe Ad 3,4,5,6,7) erweiterten wir unter Berücksichtigung einer möglichen bakteriellen pulmonalen Superinfektion als Mitursache der erneuten respiratorischen Verschlechterung das Antibiotikaspektrum auf Meropenem.
Im Rahmen eines „Unresolving ARDS“ begannen wir zudem eine Therapie mit Methylprednisolon i.v. 80 mg/Tag.
Der Gasaustausch wurde in den ersten Tagen vollständig durch die ECMO gewährleistet.
Erste Messungen der Lungencompliance am sedierten Patienten zeigten Werte unter 20 ml/cmH2O.
Nach mehreren Versuchen stellten wir eine Duo-PAP-Beatmung ein, die es ermöglichte, sehr gute Plateaudrücke (um 20 cmH2O, im Verlauf weiter sinkend) beizubehalten und gleichzeitig den Atemtrigger des Patienten zuzulassen, während die Sedierung schrittweise reduziert wurde.
Mit den gewählten Strategien zeigte der Patient einen minimalen Nutzen für die Atemmechanik mit einer Verbesserung der Lungencompliance auf etwa 27 ml/cmH2O, der Gasaustausch blieb jedoch vollständig von der ECMO abhängig. Am 08.02. führten wir ein Thorax-CT durch, um unbehandelte pulmonale Komplikationen auszuschließen: Die Untersuchung zeigte das Auftreten von Parenchymkonsolidierungen mit bronchiektatischen Veränderungen in den Unterlappen, mit Verdacht auf eine schwere organisierende Pneumonie (SOP).
Die für eine SARS-CoV-2-Infektion typischen Milchglasveränderungen waren rückläufig.
Aufgrund der radiologischen Befunde entschieden wir uns, vom 09.02. bis 19.02. zusätzlich zur Steroidtherapie eine immunmodulatorische Therapie mit Azithromycin und Spironolacton durchzuführen.
Angesichts der langen Intubationsdauer, der fehlenden kurzfristigen Aussicht auf eine Extubation sowie zur Reduktion des Totraums und zur schrittweisen Beendigung der Sedierung führten wir am 11.02.2021 eine perkutane Tracheotomie durch.
Obwohl der Eingriff ohne technische Schwierigkeiten verlief, kam es nach wenigen Stunden zu einer lokalen Blutung sowohl nach außen als auch nach innen (Aspiration von reichlich blutigem Material aus der Trachea).
Wir führten am 12.02. und anschließend am 13.02. zwei chirurgische Revisionen durch, ohne eine eindeutige Quelle für eine aktive Blutung zu finden.
Im weiteren Verlauf blieb die Blutung weiterhin vorhanden und diffus, wahrscheinlich begünstigt durch eine gleichzeitig auftretende ECMO-assoziierte Koagulopathie (siehe Ad. 7). Wir unterzogen den Patienten mehrfachen Bronchialtoiletten, um die Gerinnsel aus den Atemwegen abzusaugen, die aus der Trachealblutung resultierten.
Am 16.02. wurde aufgrund einer fast vollständigen Obstruktion der unteren Atemwege eine eingehende Bronchoskopie durch die Kollegen der Pneumologie des Ospedale Civico in Lugano erforderlich.
In der Folge beobachteten wir eine langsame und schrittweise Verbesserung der Lungencompliance mit Zunahme der Beatmungsvolumina und Verbesserung des Gasaustauschs, was eine schrittweise Entwöhnung von der ECMO-Unterstützung ermöglichte.
Am 18.02. führten wir ein erneutes Thorax-CT durch, das ein im Wesentlichen zum Vorbefund vergleichbares Lungenbild zeigte.
Trotz der langsamen radiologischen Entwicklung waren sowohl Oxygenierung als auch Ventilation adäquat und wurden vom Patienten bei minimaler ECMO-Unterstützung vollständig selbst gewährleistet.
Dies ermöglichte uns die endgültige Entfernung der v-v ECMO am 18.02. ohne periprozedurale Komplikationen.
Mit der anschließenden Beendigung der ECMO sahen wir schließlich eine vollständige Rückbildung der Koagulopathie; die Trachealblutung sistierte rasch und dauerhaft ohne weitere obstruktive Episoden.
In den folgenden Stunden hielten wir den Patienten unter druckkontrollierter Beatmung, unterbrochen von Intervallen mit druckunterstützter Spontanatmung.
Die Beatmungsvolumina waren adäquat und der Gasaustausch zufriedenstellend.
48 Stunden nach Entfernung der ECMO beobachteten wir trotz optimaler Oxygenierung eine Fehlanpassung des Patienten an die mechanische Beatmung mit progredienter und schwerer Hyperkapnie und konsequenter respiratorischer Azidose, die nicht auf Änderungen der Beatmungseinstellungen ansprach. Wir entschieden uns daher für Zyklen der Bauchlagerung vom 20.02. bis 23.02.2021, was sowohl den Kohlendioxid-Wash-out als auch die Atemmechanik verbesserte, auch dank einer besseren Sekret-Clearance mit weiterem klinischem Nutzen.
Bei Verdacht auf eine schwere organisierende Pneumonie, die sich unter den vorangegangenen Therapien nicht ausreichend gebessert hatte, entschieden wir uns nach pneumologischem Konsil für eine hochdosierte Steroidtherapie: Wir verabreichten einen Boost von 1 g/Tag Methylprednisolon vom 24.02. bis 26.02.2021 (insgesamt 3 Dosen), gefolgt von 500 mg/Tag vom 27.02.2021 bis 01.03.2021.
Das anschließende Schema ab dem 02.03. sah 0,75 mg/kg/Tag für 30 Tage vor (50 mg/Tag bis zum 01.04.21), gefolgt von einer weiteren Reduktion auf 0,50 mg/kg/Tag für weitere 30 Tage.
Ein neues Thorax-CT nach dem Methylprednisolon-Boost am 01.03.2021 zeigte eine deutliche Verbesserung des Lungenbildes mit Anzeichen einer vermuteten Erkrankung der kleinen Atemwege.
Obwohl die ersten Mobilisierungen in den Sessel aufgrund von Atemerschöpfung und vollständiger Beatmungsabhängigkeit extrem schwierig waren, wurde der Patient mit den Tagen immer autonomer und belastbarer.
Das letzte Verlaufs-CT des Thorax vom 15.03. zeigt ein im Wesentlichen stationäres Lungenbild.
Dank der eingeleiteten Therapien sehen wir eine tägliche Verbesserung der Atemmechanik und des Gasaustauschs.
Es gelang uns, die respiratorische Unterstützung schrittweise zu reduzieren, bis der Patient Spontanatmung beibehalten konnte.
Der Patient profitiert weiterhin von CPAP-Zyklen im Wechsel mit High-Flow-Beatmung.
Phonationsversuche mit einer speziellen Kanüle wurden gut toleriert, sodass wir die perkutane Tracheostomie am 23.03.2021 endgültig entfernen konnten.
Zum Zeitpunkt der Verlegung ist der Patient in Ruhe weder tagsüber noch nachts mehr von einer Sauerstofftherapie abhängig.
Gemäß Vereinbarung mit Dr. …, der zuständigen Pneumologin während des Aufenthalts, wird der Patient in der Clinica Hildebrand weiterbetreut und muss eine pneumologische Nachsorge fortsetzen.
Zu 3-4-5-6-7:
Bei Aufnahme wurde der Nasenabstrich wiederholt, der die Infektion mit SARS-CoV-2, Variante N501Y, bestätigte.
Nach Rücksprache mit den Kollegen der Infektiologie kam der Patient für weitere spezialisierte Therapien nicht infrage.
Bei Verdacht auf eine bakterielle pulmonale Superinfektion als Ursache für die erneute und rasche Verschlechterung des Patienten leiteten wir ab dem 31.01. eine Therapie mit Meropenem ein. Das Bronchialaspirat und die bei Aufnahme entnommenen Blutkulturen zeigten das Wachstum von Klebsiella pneumoniae, sensibel auf die laufende Therapie, aber resistent gegen die zuvor verabreichte Antibiotikatherapie mit Piperacillin-Tazobactam.
Die Urinkultur, die Urin-Antigene für Legionellen und Pneumokokken, die Untersuchung auf Aspergillus-Galactomannan im Bronchialaspirat und der Beta-Glucan-Test, ebenfalls am 31.01. durchgeführt, waren negativ.
Wir führten am 04.02. erneut ein Bronchialaspirat und eine CMV-Suche im Serum durch, die negativ ausfielen.
Der Entzündungsverlauf war langsam rückläufig mit sinkenden Entzündungsparametern: Wir setzten die Therapie mit Meropenem bis zum 10.02. fort und schlossen den Antibiotika-Zyklus gemäß Antibiogramm mit Ceftriaxon vom 10.02. bis 14.02.2021 ab.
Ab dem 11.02. traten Fieber und ein erneuter Anstieg der Entzündungsparameter auf: Bei Verdacht auf einen nicht sanierte Fokus wiederholten wir die Blutkulturen (12.02. und 14.02.2021) sowie Urinkulturen (12.02.2021) und führten eine bronchiolo-alveoläre Lavage durch, bei der neben der allgemeinen Bakteriologie gezielt nach Legionellen und Aspergillus-Galactomannan gesucht wurde (11.02.2021).
Wir wiederholten die CMV-Serologie zum Ausschluss einer möglichen Reaktivierung, die negativ ausfiel.
Die Antibiotikatherapie wurde erweitert, indem Ceftriaxon ab dem 15.02. durch Cefepim ersetzt wurde.
Die Kulturen zeigten ein Wachstum von Enterococcus faecalis in der BAL (11.02.2021), sensibel auf die laufende Therapie, und von Enterococcus faecium in den Blutkulturen (12.02.2021), was die Einleitung von Vancomycin gemäß Antibiogramm erforderte.
Die übrigen zwischen dem 11.02. und 14.02.2021 durchgeführten Kulturen waren negativ.
Die ventilatorassoziierte Pneumonie durch Enterococcus faecalis wurde bis zum 20.02.2021 mit Cefepim behandelt.
Hinsichtlich der Bakteriämie durch Enterococcus faecium betrachten wir die Lunge als möglichen Ausgangsfokus, auch angesichts der CT-Bilder vom 18.02., die beidseitige pulmonale Konsolidierungszonen zeigen.
Die Therapie mit Vancomycin wurde am 22.02. zugunsten von Linezolid abgesetzt, einem Antibiotikum mit besserer Penetration in das Lungengewebe.
Wir setzten die eingestellte Therapie bis zum 04.03.2021 fort.
Trotz der gezielten Therapien blieb der Patient stets subfebril mit einem stabilen Entzündungssyndrom.
Nach dem Auftreten deutlicher Fieberspitzen ab dem 19.02.2021 wiederholten wir angesichts der extremen Immunfragilität des Patienten erneut ein breites Spektrum an Kulturen: serielle Blutkulturen (19.02., 22.02., 27.02.2021), Bronchialaspirat (21.02.2021) und BAL (22.02., 28.02.2021) mit Suche nach Legionellen und Aspergillus-Galactomannan, Serologien für CMV und Strongyloides sowie Beta-Glucan-Bestimmung.
Wir behielten eine Antibiotikaprophylaxe mit Meropenem ab dem 20.02.2021 bei.
Alle durchgeführten Untersuchungen waren negativ.
Im Verlauf kam es zu einem langsamen Absinken der Entzündungsparameter, ohne jedoch jemals eine deutliche Normalisierung zu erreichen.
Die Therapie mit Meropenem wurde am 02.03.2021 beendet.
In Anbetracht der nun seit fast zwei Monaten laufenden hochdosierten Steroidtherapie, die einen effektiven Zustand der Immunsuppression bedingt, entschieden wir uns nach infektiologischem Konsil für eine Prophylaxe mit Co-Trimoxazol dreimal wöchentlich ab dem 01.03.2021.
Nach einigen Tagen ohne Fieberspitzen wurde der Patient ab dem 01.03.2021 wieder subfebril.
Die Entzündungsparameter, die nie vollständig gesunken waren, blieben stationär.
Vorsichtshalber wiederholten wir erneut die Kulturen: serielle Blutkulturen (01.03., 05.03., 07.03.2021), Urinkulturen (01.03., 05.03.2021), Bronchialaspirat (05.03., 08.03.2021), Suche nach Aspergillus-Galactomannan im Serum und Bronchialaspirat (05.03.2021) sowie CMV-Suche.
Da der Gasaustausch stets adäquat war und keine hämodynamischen Veränderungen vorlagen, die auf einen drohenden septischen Zustand hindeuten könnten, entschieden wir uns gegen eine neue Antibiotikatherapie.
Alle durchgeführten Kulturen waren negativ.
Als Ursache für den fiebrigen und entzündlichen Zustand kommt mangels klarer infektiöser Ursache eine SOP, eine pharmakologische Ursache durch die laufende Antihistaminika- und Neuroleptikatherapie (siehe Ad. 9-10), ein entzündlicher Rebound bei Reduktion der Steroidtherapie oder eine Reaktivierung der bekannten CML (siehe 13) infrage. Mit den Tagen und der gleichzeitigen Reduktion der Sedierungstherapie kam es zum spontanen und schrittweisen Verschwinden des Fiebers mit langsamer und vollständiger Normalisierung der Entzündungswerte.
Wir weisen auf die Möglichkeit hin, die Isolierung des Patienten ab dem 15.02.2021 aufzuheben, da die SARS-CoV-2-PCR im Nasenabstrich vom 09.02.2021, in der BAL vom 11.02. und im Stuhl vom 10.02.2021 negativ war und eine adäquate Antikörperabdeckung vorlag (IgG negativ und IgM positiv am 10.02.2021).
Das letzte Bronchialaspirat vom 22.03., entnommen bei einem fieberfreien Patienten ohne Entzündungszeichen, zeigte kein bakterielles Wachstum.
Zu 8:
Mit Beginn der ECMO trat sofort eine mechanische hämolytische Komponente auf, gekennzeichnet durch Anämie und Thrombozytopenie, die eine gezielte Transfusionsunterstützung erforderte. Die Antikoagulation wurde mit Liquemin bei einer aPTT um 50 Sek. aufrechterhalten.
Mit den Tagen beobachteten wir das Auftreten einer Koagulopathie mit diffusen Blutungen aus der Tracheostomie, den Mund- und Nasenschleimhäuten, das Auftreten spontaner Hämatome, Petechien an den Händen und marsalafarbenem Urin.
Angesichts extrem erhöhter D-Dimere (Maximalwert am 12.02.2021 mit 46,32 mg/l) konnten wir, auch wenn kein eindeutiger Fibrinogenverbrauch vorlag, eine disseminierte intravasale Koagulopathie nicht ausschließen.
Differentialdiagnostisch kamen eine Verbrauchskoagulopathie bei persistierenden Blutungen oder eine ECMO-induzierte Koagulopathie infrage.
Der periphere Blutausstrich schloss eine thrombotische Mikroangiopathie aus.
Obwohl keine eindeutigen fokalen Defizite vorlagen, führten wir zeitgleich mit dem Thorax-CT am 18.02.2021 ein Schädel-CT durch, das intrakranielle Blutungen ausschloss.
Mit dem Absetzen der ECMO-Unterstützung sistierten die Blutungen spontan innerhalb weniger Stunden.
Im weiteren Verlauf traten keine Rezidivblutungen auf, und wir setzten die Antikoagulation mit Liquemin im therapeutischen Bereich fort.
Angesichts des anschließenden deutlichen Abfalls der D-Dimere und des Entzündungssyndroms führten wir ab dem 17.03.2021 nur noch eine Prophylaxe durch.
Hämoglobin und Thrombozyten blieben stabil mit einem Entlassungswert von 92 g/dl bzw. 153 G/l.
Zu 9-10-11:
Bei Aufnahme auf die Intensivstation war eine multimodale Sedierung erforderlich, um eine adäquate Anpassung an das Beatmungsgerät zu gewährleisten.
Die täglichen neurologischen Beurteilungen ermöglichten den Ausschluss fokaler Defizite und gewährleisteten einen guten Komfort für den Patienten.
Nach Überwindung der akuten Phase und Entfernung der ECMO-Unterstützung reduzierten wir schrittweise die Sedierung.
Es zeigte sich sofort ein hyperkinetisches Delir mit Unruhe, Angst, Beatmungsdiskordanz sowie schwerer nächtlicher und täglicher Schlaflosigkeit.
Wir titrierten schrittweise die neuroleptische und sedative multimodale Therapie (Benzodiazepine, Neuroleptika, Antihistaminika); in den ersten Tagen profitierte der Patient von einer Sedierung zunächst mit Propofol und dann mit nächtlichem Dexdor.
Mit den gewählten Strategien kam es zu einer langsamen und schrittweisen klinischen Besserung: Der Patient nahm wieder einen regelmäßigen Tag-Nacht-Rhythmus auf, war gut kooperativ und motiviert. Die eingestellte Therapie wurde schrittweise reduziert und den Bedürfnissen des Patienten angepasst.
Eine schwere Intensivstation-Myopathie trat rasch aufgrund der erzwungenen Bettlägerigkeit unter ECMO, der zahlreichen infektiösen Komplikationen und der katabolen hochdosierten Steroidtherapie auf.
Nach Absetzen der ECMO wirkte der Patient kachektisch mit einer schweren Muskelatrophie, die einen Zustand der Tetraplegie bedingte.
Dank der rasch eingeleiteten Physiotherapie konnte der Muskeltonus teilweise wiedererlangt werden: Eine eigenständige Mobilisierung der proximalen Muskulatur und eine diskrete Rumpfkontrolle sind möglich, die periphere und Feinmotorik sind noch nicht wiederhergestellt.
Der Transfer in den Sessel ist mit Hilfsmitteln möglich.
Auch die Atemmuskulatur gewann schrittweise so viel Kraft zurück, dass die Tracheostomie am 24.03.2021 entfernt werden konnte.
Wir setzen die Atemphysiotherapie mit Erfolg fort.
Eine am 11.03.2021 zu prognostischen Zwecken durchgeführte Elektroneuromyographie zeigt lediglich eine beginnende peripher-distale neuropathische Komponente im Bereich der Nervi peronei beidseits; das restliche Bild bleibt vereinbar mit einer Myopathie infolge des kritischen Zustands und der verlängerten Kortisontherapie.
Mit der Wiederaufnahme der eigenständigen Mobilisierung zeigt sich ein diffuser Myoklonus/Opisthotonus, insbesondere im Bereich der Gesichtsmuskulatur, der Zunge und der oberen Extremitäten.
Nach neurologischem Konsil leiteten wir eine Therapie mit Keppra ein und führten ein Schädel-MRT durch, das eine postanoxische oder ischämische Form ausschloss.
Eine postinfektiöse Form ist möglich; angesichts des aktuellen Immunsuppressionszustands und der Besserung unter der eingeleiteten Therapie sehen wir von einer Lumbalpunktion zum Ausschluss paraneoplastischer oder autoimmuner Formen ab.
Das Zittern bessert sich unter der eingeleiteten Therapie schrittweise, eine intentionale Komponente bleibt bestehen.
Wir überlassen den Kollegen der Hildebrand-Klinik die Optimierung der Therapie und eventuelle weitere Abklärungen.
Zu 12:
Der Patient erhielt ab Aufnahme eine enterale Ernährung mit kalorischem Zielwert über eine Nasogastralsonde (NGS).
Eine in den ersten Tagen der Wiederernährung aufgetretene Hypophosphatämie wurde rasch korrigiert.
Das Abdomen war stets ruhig mit Stuhlgang von geformter Konsistenz.
Angesichts der offensichtlichen multifaktoriellen Malnutrition und der schweren Intensivstation-Myopathie sowie im Bewusstsein des hohen Dysphagierisikos unterzogen wir den Patienten am 15.03.2021 einem logopädischen Konsil, das den klinischen Verdacht bestätigte.
Dank der Fortführung der Physiotherapie und der Durchführung gezielter logopädischer Übungen besserte sich die Dysphagie schrittweise, und wir konnten auf passierte Kost umstellen. Nach Entfernung der Tracheostomie besteht weiterhin ein gutes Schluckvermögen ohne Anzeichen einer Dysphagie, was die Entfernung der NGS und die Wiederaufnahme einer normalen Diät ermöglicht.
Zu 13:
Der Patient ist für eine chronische myeloische Leukämie unter Imatinib-Therapie bekannt.
Bei Aufnahme entschieden wir uns unter Berücksichtigung des Risikos einer pulmonalen Toxizität der Therapie in Absprache mit dem behandelnden Hämatologen für das Absetzen des Chemotherapeutikums.
Das Wiederauftreten eines Entzündungssyndroms und von Fieberspitzen ab dem 01.03.2021 bei Fehlen eines eindeutigen infektiösen Fokus begründete den klinischen Verdacht auf eine Reaktivierung der Erkrankung.
Auf hämatologischen Rat hin führten wir einen peripheren Blutausstrich durch, der das Vorhandensein zirkulierender Blasten ausschloss.
In Anbetracht der guten klinischen Stabilität und des schrittweise günstigen Verlaufs entschieden wir uns in Absprache mit dem behandelnden Hämatologen für die Wiederaufnahme der Imatinib-Therapie ab dem 12.03.2021.
Am 25.03.2021 verlegen wir Herrn Achermann auf die Station in Erwartung der Verlegung in die Clinica Hildebrand.
Weiteres Vorgehen:
- Verlegung in die Clinica Hildebrand in einer Woche je nach Verfügbarkeit planen;
- Ab dem 01.04.2021 Fortführung mit Prednison 30 mg/Tag, anschließendes Tapering mit der behandelnden Pneumologin Dr. … zu besprechen;
- Fortführung der Bactrim-Prophylaxe bis zur pneumologischen Neuevaluation;
- Fortführung der eingestellten neurologischen Therapie mit Keppra, Neuevaluation von Therapieänderungen oder eventuellen weiteren Abklärungen je nach Entwicklung des Tremors mit den Kollegen der Hildebrand-Klinik;
- Fortführung der Atemphysiotherapie und Mobilisierung;
- Gemäß Anforderung von Dr. …, der behandelnden Hämatologin, Bestimmung von BCR/ABL1 im Blut zur Überwachung der bekannten CML vorsehen.
Therapie bei Entlassung:
Siehe computerisierte Patientenakte Whale.
Wir stehen für Rückfragen zur Verfügung und verbleiben mit freundlichen Grüßen.
Prof. Dr. med. …
Dr. med. …
Dr. med. …